今天,分享一篇《生物精神病学》吃东西抗焦虑?不,“饿着”才行!,希望以下《生物精神病学》吃东西抗焦虑?不,“饿着”才行!的内容对您有用。
俗话说,没有什么是一顿火锅解决不了的,如果有,那就再加一顿烤肉!
有科学依据吗?不知道。
反正在奇点糕的潜意识里,烦躁不安的时候吃点东西,心情就能一整个阴转晴。以前总吹嘘吃美食缓解焦虑情绪这一招屡试不爽,但近期发表在《生物精神病学》杂志上的一项研究结果却颠覆了本糕的认知……
瑞典哥德堡大学的Karolina P. Skibicka团队发现,进食与选择性化学激活肠道支配的迷走神经传入神经元,均能增加雄性和雌性大鼠的类焦虑行为;相反,化学抑制肠道迷走神经传入神经元,便会阻断进食诱导的类焦虑行为。
具体来说,胃肠道迷走神经感觉信号是大鼠通过中央杏仁核(CeA)调节类焦虑行为的关键,如果基于胃肠道迷走神经的肠-脑神经反馈长期中断,雄性大鼠的类焦虑行为则会明显减少,而雌性大鼠的类焦虑行为变化不大,即肠-脑神经反馈受损对类焦虑行为的影响具有性别差异[1]。
 论文首页截图
论文首页截图大脑适应性感知身体内部状态的能力被称为内感受。有研究表明,内感受功能失调是焦虑症病因的一个组成部分[2],阐明内感受的神经机制及其在焦虑症中功能失调的具体通路,对治疗焦虑症至关重要。
内感受调节的一个显著例子就是:小鼠在光照结束(摄入每日大部分热量之前)阶段表现出的类焦虑行为比光照开始时要少,而且与自由进食相比,禁食或限制热量摄入减少了小鼠的类焦虑行为[3-6]。
也就是说,小鼠进食与类焦虑行为增加有关。虽然观察到了这一现象,然而,胃肠道中进食相关的代谢信号如何到达大脑,并促使大脑产生类焦虑行为的神经反馈仍然尚未阐明。
针对上述问题,Skibicka团队选择啮齿类动物——大鼠作为实验对象,设计了两种进食状态:夜间禁食或1小时自由进食,并采用4种测试来评估进食状态对大鼠类焦虑行为的影响,分别为高架十字迷宫测试、旷场实验、听觉惊跳反射实验及食物恐新症测试。
结果显示,在旷场测试中,进食大鼠比禁食大鼠进入中心区域的行走距离更短、频率更低,但总的行走距离没有显著差异。在高架十字迷宫测试中,进食大鼠比禁食大鼠张开双臂行走的距离和时间均明显缩短,但总距离没有减少。
此外,与禁食的大鼠相比,进食大鼠在自发活动独立测试中表现出更高的听觉惊跳反射,并且对进食新食物的延迟更长。

与禁食相比,自由进食增加了雄性和雌性大鼠的类焦虑行为
上述结果表明,进食状态可调节类焦虑行为,自由进食增加了雄性和雌性大鼠的类焦虑行为,并且与运动或饥饿的变化无关。
考虑到胃肠道牵拉反射与营养来源的信号可激活迷走神经传入神经元[7],接下来研究人员便采用双重病毒注射策略,探究了大鼠胃和十二指肠迷走神经传入神经元的激活是否会增加大鼠类焦虑行为。
研究人员向大鼠腹腔注射氯氮平N-氧化物(CNO),作为化学刺激以激活胃肠道迷走神经的传入神经元,在表达hm3d(Gq)的大鼠中,注射CNO显著减少了大鼠1小时的食物摄入量,而在不表达hm3d(Gq)的对照大鼠中则没有。
研究结果显示,肠道支配的迷走神经传入神经元经化学激活后,大鼠在旷场中心区域的移动距离明显缩短;在高架十字迷宫测试中,大鼠张开双臂行走的距离大大缩短;开始进食的时间也有所延迟。但大鼠对听觉刺激的惊跳振幅并没有明显变化,说明其不受迷走神经传入神经元的激活调节。
这些结果表明,选择性激活胃和十二指肠迷走神经的传入神经元,可诱导大鼠产生类焦虑行为。
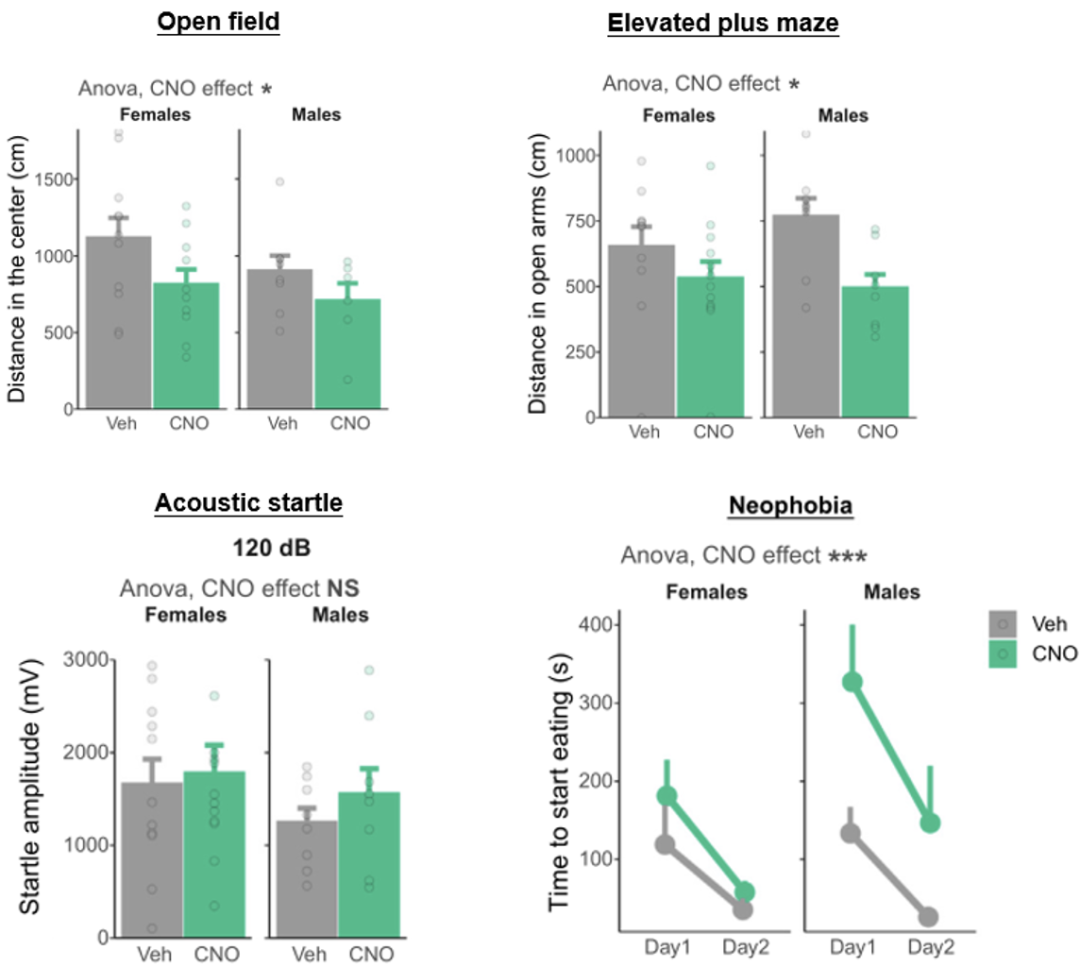
化学激活胃肠道迷走神经传入神经元,增加了雄性和雌性大鼠的类焦虑行为
既然进食和肠道迷走神经传入神经元的选择性激活均能增加雄性和雌性大鼠的类焦虑行为,那么肠道迷走神经的传入神经元对进食诱导的焦虑效应是否是必要的呢?
研究人员同样采用双重病毒注射策略,但表达的是抑制性DREADD受体,以探究选择性抑制肠道迷走神经传入神经元对进食诱导的焦虑效应的影响。
结果显示,化学抑制肠道迷走神经传入神经元后,进食组大鼠在旷场测试中进入中心区域的行走距离,以及在高价十字迷宫中张开双臂行走的距离和时间均明显增加,但禁食组大鼠并未受影响。
在自发活动独立测试中,化学抑制肠道支配的迷走神经传入神经元后,进食组大鼠对听觉刺激的惊跳反应有所减弱,对进食新食物的延迟明显缩短,而禁食组大鼠依然未受影响。
这些结果表明,肠-脑迷走神经反馈对进食诱导的类焦虑行为是必要的。
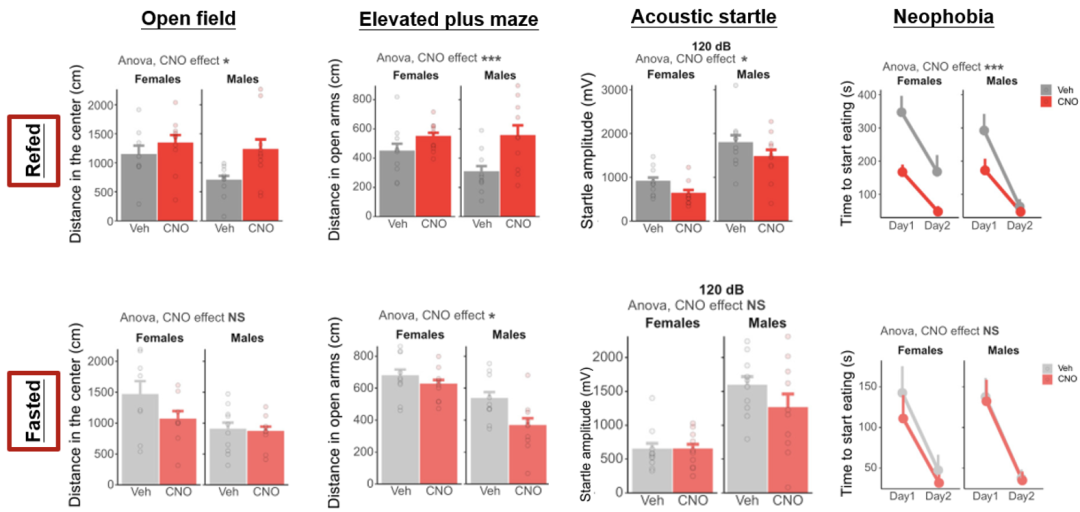
化学抑制肠道支配的迷走神经传入神经元阻断了再喂食诱导的焦虑效应
问题又来了!从胃肠道到大脑的迷走神经反馈如果发生损伤,是否会导致类焦虑行为的持续变化呢?
研究人员向大鼠双侧迷走神经结状节内注射CCK-SAP以抑制Cckar表达,结果表明,长期中断胃肠道迷走神经反馈可减少雄性大鼠的类焦虑行为,但对雌性大鼠没有影响,说明肠-脑迷走神经反馈对类焦虑行为的调节具有性别差异。
插播一条,化学选择性抑制迷走神经传入神经元后,雌性与雄性大鼠类焦虑行为的变化并没有明显差异,怎么中断迷走神经反馈回路后,大鼠的类焦虑行为变化就表现出性别差异了呢?
其实是因为雄性大鼠CeA中与抗焦虑型相关的转录基因组发生了改变,而这些改变在雌性大鼠中却不存在(或大大减弱)。
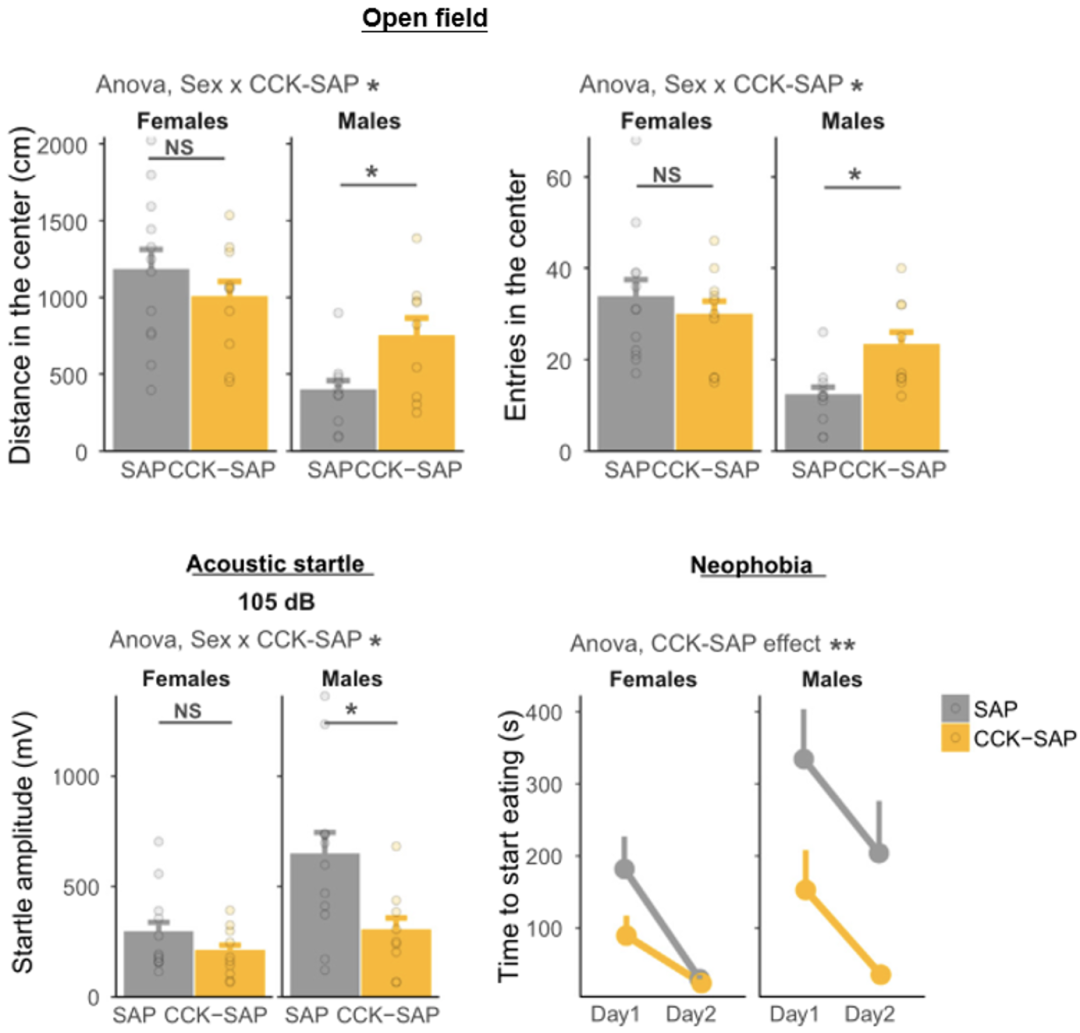
长期胃肠道迷走神经传入神经元损伤以性别依赖的方式减少类焦虑行为
进一步研究发现,与进食相关的迷走神经信号主要影响CeA,引发进食状态变化诱导的焦虑效应,而且雄性大鼠中CCK-SAP的抗焦虑作用与杏仁核中γ-氨基丁酸(GABA,中枢神经系统抑制性神经递质)信号增强有关。
随后研究人员将GABAA受体拮抗剂Bicuculline注入雄性CCK-SAP大鼠或相应对照大鼠的CeA中,并通过听觉惊跳反射测试它们的类焦虑行为。Bicuculline显著增加了CCK-SAP大鼠对105分贝刺激的惊跳幅度,但并未对对照组大鼠产生影响,这表明胃肠道迷走神经传入神经元调节的类焦虑行为是由雄性大鼠CeA中的GABA信号介导的。
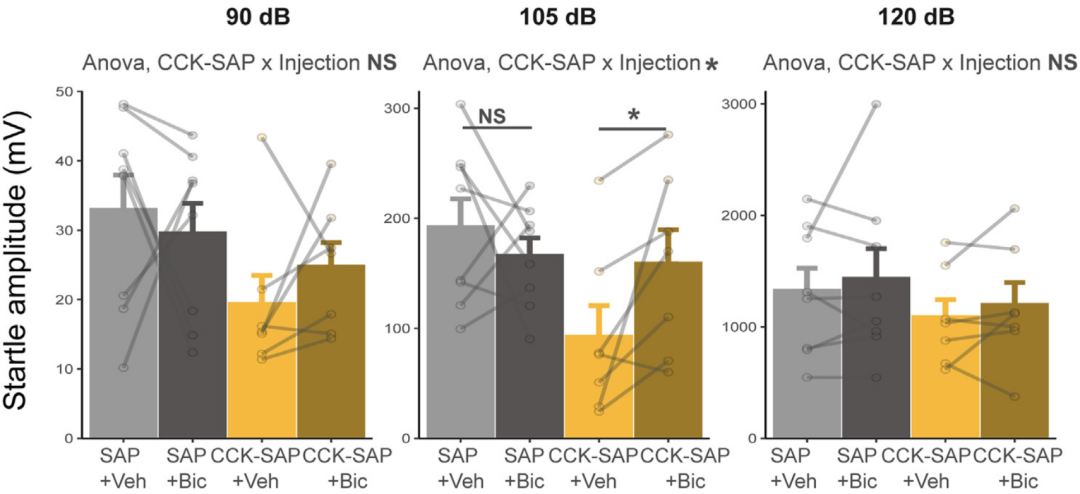
CCK-SAP雄性大鼠对声音刺激的惊跳振幅
总的来说,这项研究采用化学遗传学、神经药理学和行为学等多种方法,明确揭示了胃肠道迷走神经传入神经元在焦虑调节中的作用。
Skibicka团队指出,胃肠道的迷走神经感觉信号对大鼠通过CeA调节的类焦虑行为至关重要,肠道迷走神经的传入神经元神经元可根据进食状态不同调整类焦虑行为,为进食诱导的焦虑效应提供了肠-脑神经反馈。而且,长期中断该神经反馈对类焦虑行为的影响具有性别差异性。
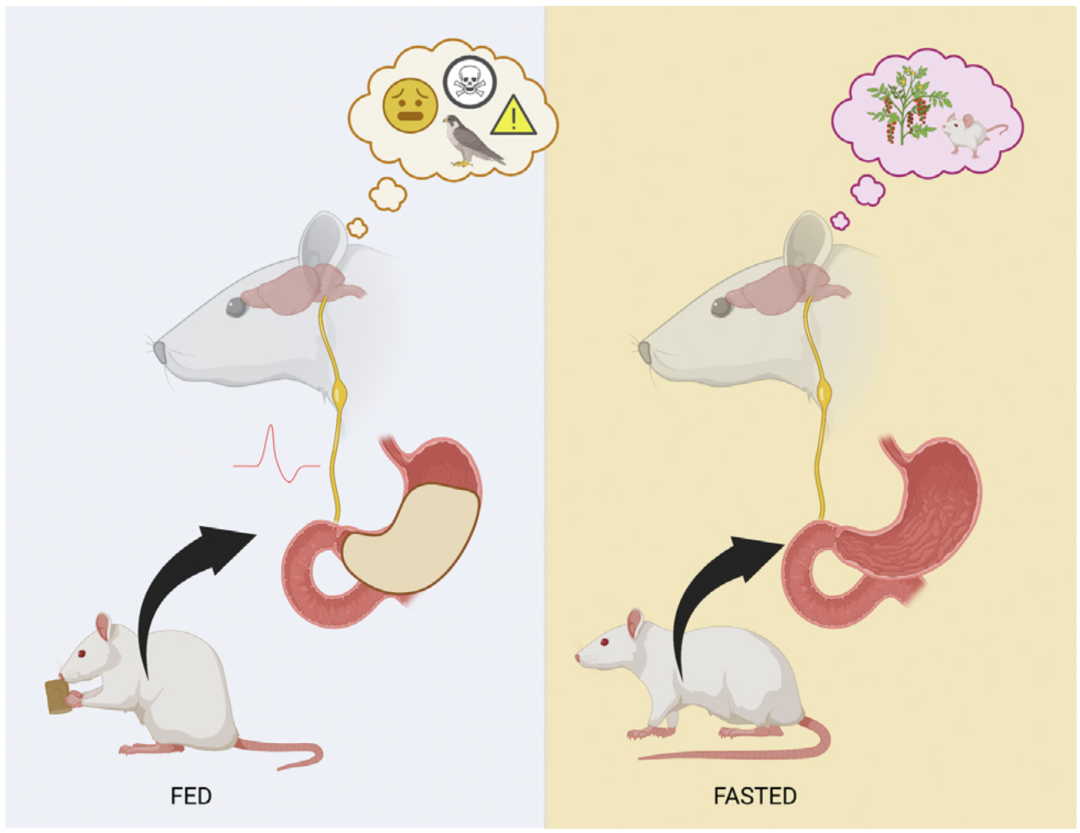 机制示意图
机制示意图基于以上研究结果,Skibicka团队提出了一个新的问题:肠-脑迷走神经反馈的中断,即内感受功能失调,是否是导致焦虑症患者对躯体感觉具有高度敏感性和高度警惕性的潜在机制呢?这当然需要进一步的研究才能证实,但如果是这样,那么靶向迷走神经肠-脑信号便有望成为焦虑症患者胃肠道内感受功能正常化的治疗手段。
最后,奇点糕只想感叹一句,健康的身心终究逃不过少吃一顿哇~
来自:奇点神思