▎药明康德内容团队编辑
我们身体中的微生物无时无刻不影响着生理功能,越来越多的证据显示包括肠道菌在内的微生物在多方面调控着我们的生理行为,甚至能够通过胃肠道迷走神经向大脑传输特定信号。在肿瘤学领域,微生物也是科学家重点关注的对象之一。
目前大多数研究发现的是,微生物存在调控癌症易感性和肿瘤进展的现象。它们通常不会直接发挥作用,而是通过影响一些代谢和免疫系统的信号通路来影响肿瘤发生,并且作用的一般都是临近的肿瘤组织。
随着测序技术的发展,以色列和美国的部分科学家已经表明,微生物不仅仅是间接影响肿瘤,更可能是肿瘤的一部分。今天,西湖大学生命科学学院蔡尚课题组在《细胞》发文,不仅再次确认肿瘤中存在细菌的事实,并且首次证明乳腺癌中独特的胞内菌在肿瘤转移定植中起着关键作用。
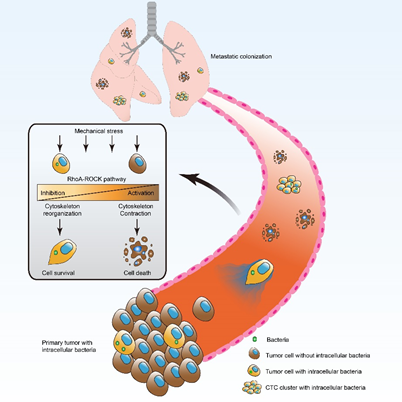
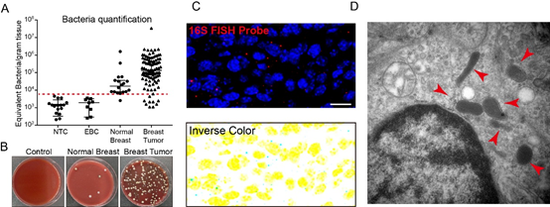
在新研究中,蔡尚博士和同事构建了一批乳腺癌模型小鼠,这些癌细胞组织充满了大量细菌,有点类似于人类乳腺癌中观察的现象。直观来看,乳腺癌组织中的细菌数量大约为正常乳腺组织中的10倍。
更令人惊讶的是,这些细菌许多都定植于癌细胞的胞液中,也就是细胞内部。这些癌细胞内的细菌甚至是存活状态,并且会在细胞渗透性的抗生素环境中逐渐死亡。
他们观察到,当癌细胞在循环系统中到处游荡时,这些细菌也会随之一同在身体各处穿行。这些细菌似乎能够调节细胞的肌动蛋白网络,并且帮助癌细胞迁移过程中应对机械性压力,提高存活率。
在研究测试中,癌细胞中的细菌似乎专门帮助癌细胞进行转移,而对原位瘤的生长影响不大。通过向小鼠尾静脉注射复合抗生素,他们尝试特异性地对肿瘤菌群进行了清除。当肿瘤菌群被清除后,肿瘤本身的体积并没有因此缩小,但肺部转移瘤明显减少,这说明这些细菌对肿瘤转移非常关键。
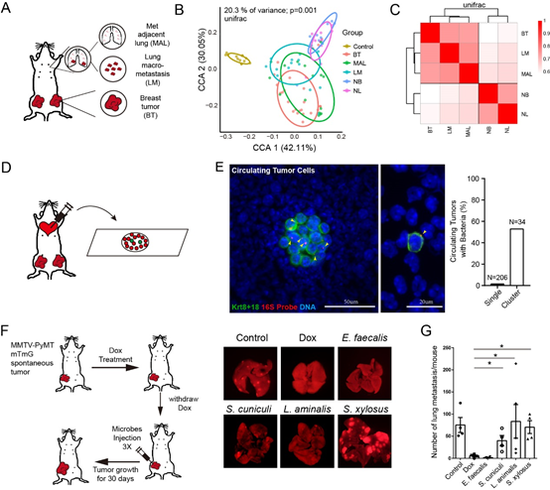
研究设法收集了在外周血中的肿瘤菌群,当这些细菌回输到肿瘤小鼠体内后,肿瘤原位的生长过程几乎没有影响,但是肿瘤转移水平开始显著增加,甚至很少发生转移的肿瘤类型也会开始出现大量转移。
而细菌在转移中做的最重要的一件事就是帮助癌细胞抵抗机械性压力,常规来说,癌细胞随着血液移动,很容易受到一种称作液流剪切压力的机械力影响而死亡。但细菌能够重塑细胞骨架,增强抵抗液流压力的能力,让肿瘤转移起来更轻松。
这种“共生”的关系实在非常惊人,似乎细菌寄宿在了肿瘤内,然后又帮助了肿瘤转移。研究通讯作者蔡尚博士告诉我们,关于肿瘤内为何富集细菌,以及细菌的来源还不清楚,这可能与肿瘤的免疫抑制环境有关,但是也可能涉及更为复杂的机制,例如肿瘤的非生物环境、代谢环境等。
尽管研究已经确认胞内菌在癌转移中发挥重要作用,但研究团队并不排除这些细菌影响原位癌症进展的可能性。
我们可能更加关心,有了这一研究是否能够帮助我们抵御和治疗肿瘤?蔡尚博士指出,目前已经有一些研究提示血液里的菌群信息可以帮助诊断肿瘤发生,利用血液菌群判断癌转移是未来非常值得探索的方向。
研究团队希望未来能在临床层面收集肿瘤菌群与肿瘤进展关系的证据,开发调控肿瘤菌群的新方法,探索肿瘤菌群与肿瘤互作的深层机制。
蔡尚课题组的研究主要以乳腺为模式器官,探讨乳腺干细胞在青春期、孕期、哺乳期对乳腺特定结构功能的维持,以及乳腺癌干细胞在癌症的发生、发展、抗药性、复发及转移过程中的重要作用。近期的研究开辟了肿瘤菌群生理功能的新肿瘤研究方向,是一个充满未知的新兴领域,期待有兴趣探讨肿瘤菌群的优秀博后的加入,共同解开微生物与癌细胞互作之谜。
实验室网页:https://www.cai-lab.com
参考资料:
[1] Evidence in mice that bacteria in tumors help cancer cells metastasize。 Retrieved Apr 7th, 2022 from https://www.eurekalert.org/news-releases/948302
[2] Aikun Fu , B。 et al。 Tumor-resident intracellular microbiota promotes metastatic colonization in breast cancer。 Cell (2022), DOI: 10.1016/j.cell.2022.02.027
[3] Nejman, D。 et al。 The human tumor microbiome is composed of tumor type-specific intracellular bacteria。 Science 368, 973-980, doi:10.1126/science.aay9189 (2020)。
[4] Riquelme, E。 et al。 Tumor Microbiome Diversity and Composition Influence Pancreatic Cancer Outcomes。 Cell 178, 795-806 e712, doi:10.1016/j.cell.2019.07.008 (2019)。
[5] Jin, C。 et al。 Commensal Microbiota Promote Lung Cancer Development via gammadelta T Cells。 Cell 176, 998-1013 e1016, doi:10.1016/j.cell.2018.12.040 (2019)。