原标题:强生新冠疫苗III期研究成功,计划2月初申请紧急使用授权
大健康
作者:林怡龄
编辑:刘聪
1 分钟前
[亿欧导读]
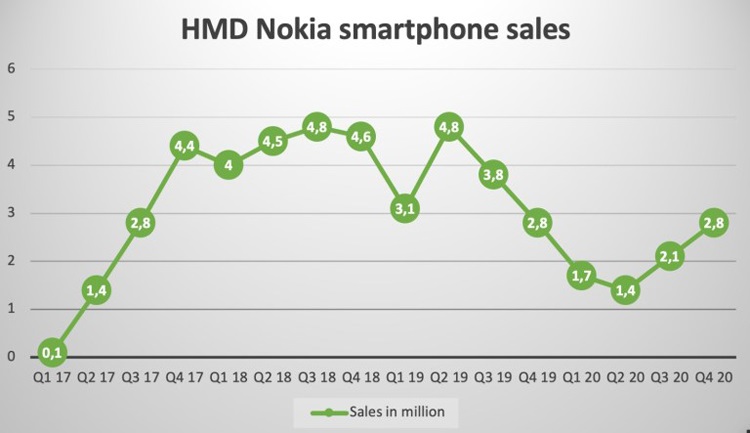
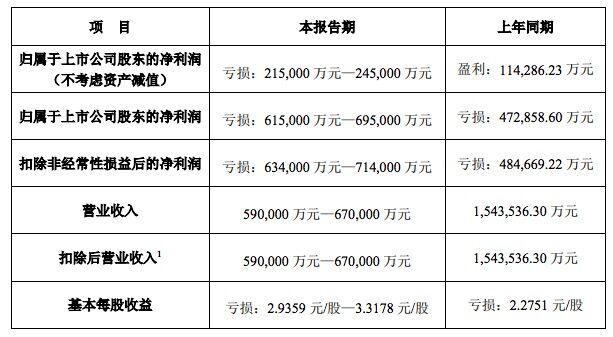
该款疫苗预防中、重度COVID-19的总体有效率达到66%。
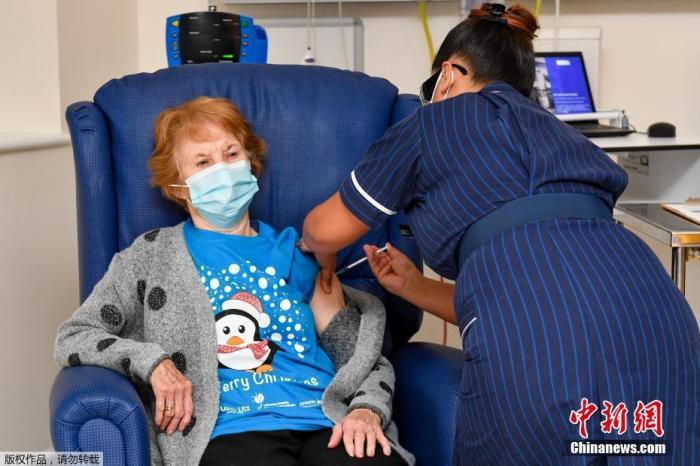
 题图来自“收费图库”
题图来自“收费图库”美国时间29日,强生宣布其在研单剂新冠疫苗(JNJ-78436735)在代号为ENSEMBLE的III期临床研究中达到所有主要临床终点和关键次要终点,并计划于2月初向FDA提交紧急使用授权申请。
据悉,JNJ-78436735新冠候选疫苗为强生采用其AdVac疫苗平台开发,该平台曾还用于开发和生产此前获得欧盟委员会批准的埃博拉疫苗。此外,该平台也开发过寨卡病毒、RSV和艾滋病毒候选疫苗。
强生官网显示,此次新冠候选疫苗临床研究的安全性和有效性数据是基于43783名受试者,其中有468例出现有症状的新冠感染。在对这些数据进行分析后发现,单次接种28天后,该款疫苗预防中、重度COVID-19的总体有效率达到66%。值得注意的是,不同地区保护效力有所不同,美国为72%,拉丁美洲为66%,南非为57%。
而在此次临床研究中,ENSEMBLE的研究结果还包含了对新出现的冠状病毒毒株的疗效。研究显示,所有变种和研究区域(包括南非,几乎所有COVID-19病例(95%)感染了B.1.351突变株)保护效力普遍一致。
另外,疫苗对所有地区重度COVID-19预防效力达到了85%,且预防效果随时间增强。接种疫苗49天后,已无重度COVID-19病例报告。而在安全性方面,对不良事件的回顾表明,疫苗耐受性良好。
强生指出,公司将对ENSEMBLEIII期临床研究的参与者进行长达两年的持续随访,以评估安全性和有效性,并将不断分析以更新数据。强生表示,将在2月初向FDA提交紧急使用授权,并计划在获得授权后立即分发。
据悉,其单剂疫苗可在-20°C(-4°F)保持稳定两年,在2-8℃(36 F-46 F)的温度下保存至少3个月。强生表示将使用目前用于运输其他创新药物的冷链技术运输疫苗。
本文来源于亿欧,原创文章,作者:林怡龄。转载或合作请点击转载说明,违规转载法律必究。
强生疫苗事件